本试验方法所用试剂和水,除特殊注明外,均指分析纯试剂和GB/T 6682中规定的二级水,所述溶液如未指明溶剂,均系水溶液。2.1 乙酸铵溶液[c(CH₃COONH₄)=1mol/L,pH7.0]
称取乙酸铵(CH₃COONH₄)77.09g溶于950 mL水中,用(1+1)氨水溶液和稀乙酸调节至pH7.0,加水稀释到1L,摇匀。 2.2 (1+1)氨水溶液
2.3 (1+1)盐酸溶液
2.4 氯化锶溶液[ρ(SrCl₂ 6H₂O)=30 g/L]
称取氯化锶(SrCl₂·6H₂O)30g溶于水,用水稀释到1L,摇匀。
2.5 pH10缓冲溶液
称取67.5g氯化铵溶于无二氧化碳水中,加入新开瓶的570mL浓氨水(ρ=0.090 g/mL),用水稀释至1L,贮存于塑料瓶中,并注意防止吸收空气中的二氧化碳。
2.6钙标准贮备溶液[ρ(Ca)=1g/L]
称取2.4972g经110℃烘4h的碳酸钙(CaCO₃,基准试剂)于250 mL高型烧杯中,加少许水,盖上表面皿,小心从杯嘴处加入100 mL(1+1)盐酸溶液溶解,待反应完全后,用水洗净表面皿,小心煮 沸赶去二氧化碳,无损将溶液移入1L容量瓶中,用水稀释至刻度,摇匀。
2.7钙标准溶液[ρ(Ca)=100 mg/L]
吸取10.00mL钙标准贮备溶液于100 mL容量瓶中,用水稀释至刻度,摇匀。此溶液含钙(Ca)100 mg/L。
2.8镁标准贮备溶液[ρ(Mg)=0.5g/L]
称取0.5000g金属镁(光谱纯)于250mL高型烧杯中,盖上表面皿,小心从杯嘴处加入100 mL(1+1)盐酸溶液溶解,用水洗净表面皿,无损将溶液移入1L容量瓶中,用水稀释至刻度,摇匀。
2.9镁标准溶液[p(Mg)=50 mg/L]
吸取10.00mL镁标准贮备溶液于100 mL容量瓶中,用水稀释至刻度,摇匀。此溶液含镁(Mg)50 mg/L。
2.10 K-B指示剂
称取0.5g酸性铬蓝K和1.0g萘酚绿B(C₃₀H1₅N₃Na₃Fe)与100g经105℃烘干的氯化钠一同研细磨匀,越细越好,贮于棕色瓶中。
3.1试液制备
称取2.00 g(质地轻的土壤称5.00g)通过2mm筛孔的风干试样于100 mL离心管中,沿离心管壁 加入少量乙酸铵溶液,用橡皮头玻璃棒搅拌土样,使成为均匀的泥浆状。再加入乙酸铵溶液至总体积约60 mL,并充分搅拌均匀。用乙酸铵溶液洗净橡皮头玻棒,溶液收入离心管内。
将离心管成对放在粗天平的两盘上,加乙酸铵溶液使其平衡。将平衡好的离心管对称放入离心机中,离心3min~5min,清液收集在250mL容量瓶中。如此用乙酸铵溶液处理2次~3次,直至浸出液中无钙离子反应为止[检查钙离子:取5mL浸出液于试管中,加1mL pH10缓冲溶液,再 加少许K-B指示剂,如呈蓝色,表示无钙离子,如呈紫红色,表示有钙离子]。最后用乙酸铵溶液定容。
3.2测定
吸取20.00mL试液于50mL容量瓶中,加入5.0 mL氯化锶溶液,用乙酸铵溶液稀释至刻度,摇匀。直接在原子吸收分光光度计上按钙、镁的测定要求调节仪器进行测定。读取吸光度或浓度值。
3.3绘制标准曲线
3.3.1钙、镁混合标准系列溶液[其中含钙0mg/L~10mg/L,含镁0 mg/L~4 mg/L]
分别吸取0mL、2.00mL、4.00 mL、6.00mL、8.00 mL、10.00 mL含钙(Ca)100 mg/L的标准溶液于6个100mL容量瓶中;另分别吸取0mL、1.00 mL、2.00mL、4.00 mL、6.00 mL、8.00mL含镁(Mg)50 mg/L的标准溶液于上述相应容量瓶中,各加入10.00 mL氯化锶溶液,用乙酸铵溶液稀释至刻度,摇匀。即为含钙(Ca)0.00mg/L、2.00mg/L、4.00mg/L、6.00mg/L、8.00mg/L、10.00 mg/L和含镁(Mg)0.00mg/L、0.50mg/L、1.00mg/L、2.00mg/L、3.00mg/L、4.00mg/L的钙、 镁混合标准系列溶液。
3.3.2绘制标准曲线
在原子吸收分光光度计上,与试液同条件测定。读取吸光度绘制标准曲线或求出一元直线回归方程,再计算浓度值,或从仪器上直接读取浓度值。
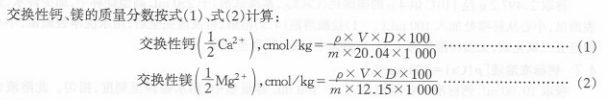
式中:
ρ——从标准曲线上查得测读液的钙(或镁)浓度,单位为毫克每升(mg/L);
V——测定液体积,单位为毫升(mL),本方法为50 mL;
D ——分取倍数,D=浸出液总体积/吸取浸出液体积=250/20;
20.04 ——钙(1/2Ca²+)离子的摩尔质量,单位为克每摩尔(g/mol);
12.15——镁(1/2Mg²+)离子的摩尔质量,单位为克每摩尔(g/mol);
1000 ——将mL换算成L的系数;
m ——风干试样质量,单位为克(g)。
重复试验测定结果以算术平均值表示,保留一位小数。